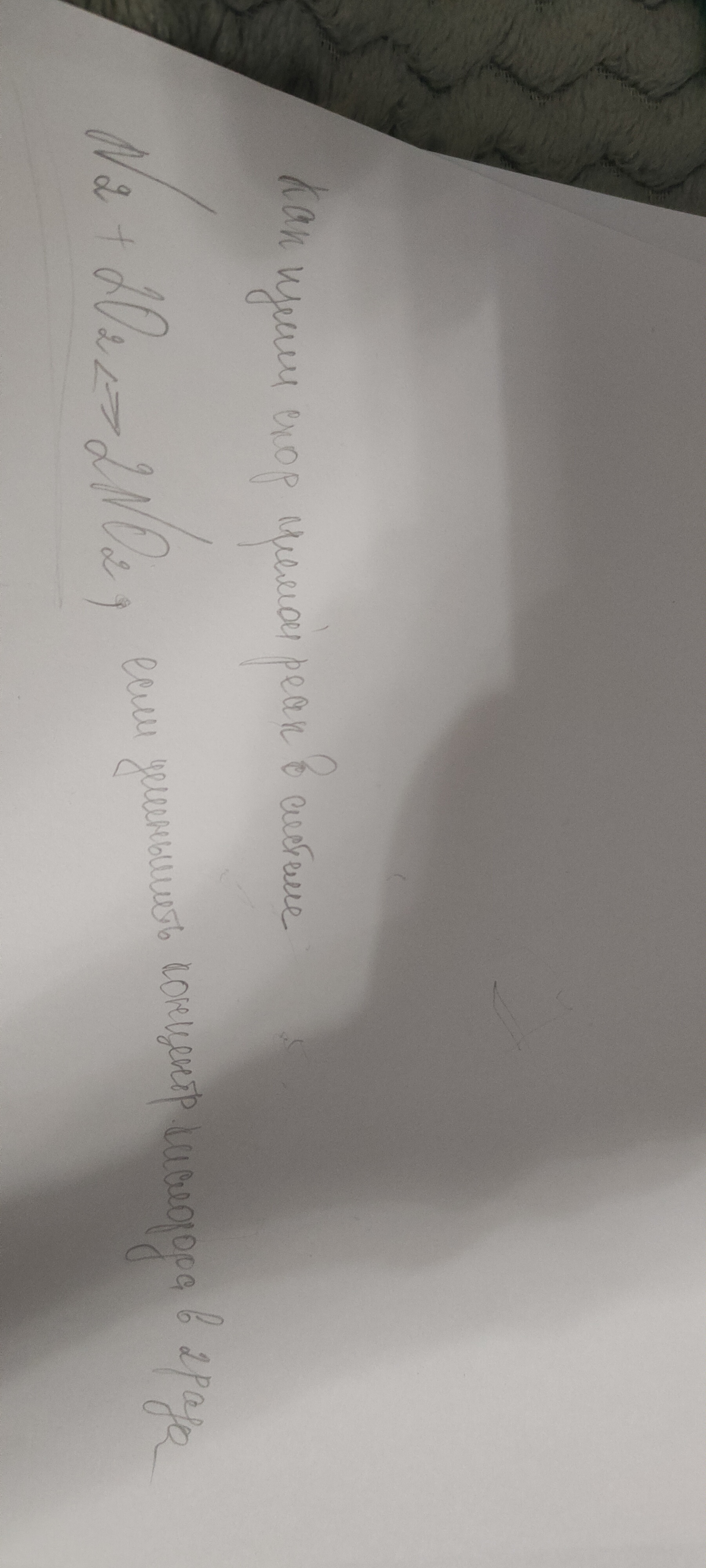Лучшие помощники
- Megamozg 2205 б
- Matalya1 1800 б
- DevAdmin 1720 б
- arkasha_bortnikov 900 б
- Dwayne_Johnson 870 б
Скорость реакции уменьшится
Согласно кинетическому уравнению V=k ∙ [O2]
при уменьшении концентраций O2 в 2 раза получим:
V2=k∙ [½O2] = k∙½ ∙ [O2] = 1/2 V
т.е. скорость реакции уменьшится в 2 раза.
Согласно кинетическому уравнению V=k ∙ [O2]
при уменьшении концентраций O2 в 2 раза получим:
V2=k∙ [½O2] = k∙½ ∙ [O2] = 1/2 V
т.е. скорость реакции уменьшится в 2 раза.
1
·
Хороший ответ
3 февраля 2023 12:50
Остались вопросы?
Еще вопросы по категории Химия
Все произношения химических символов таблицы менделеева...
Найти массу пищевой соды, которую нужно прокалить для получения 5,3 г твердого остатка....
Какое формула выражает закон Гука...
Укажите массу глицерона содержащего а) 0,9 моль кислорода б) 3,01•10²² атомов гидрогена в) 7,2 карбона...
HNO3+HCL= решить уравнение и расставить коэффициенты, а также определить окислитель и восстановитель...