Лучшие помощники
- Megamozg 2205 б
- Matalya1 1800 б
- DevAdmin 1720 б
- arkasha_bortnikov 900 б
- Dwayne_Johnson 870 б
2 апреля 2023 12:51
989
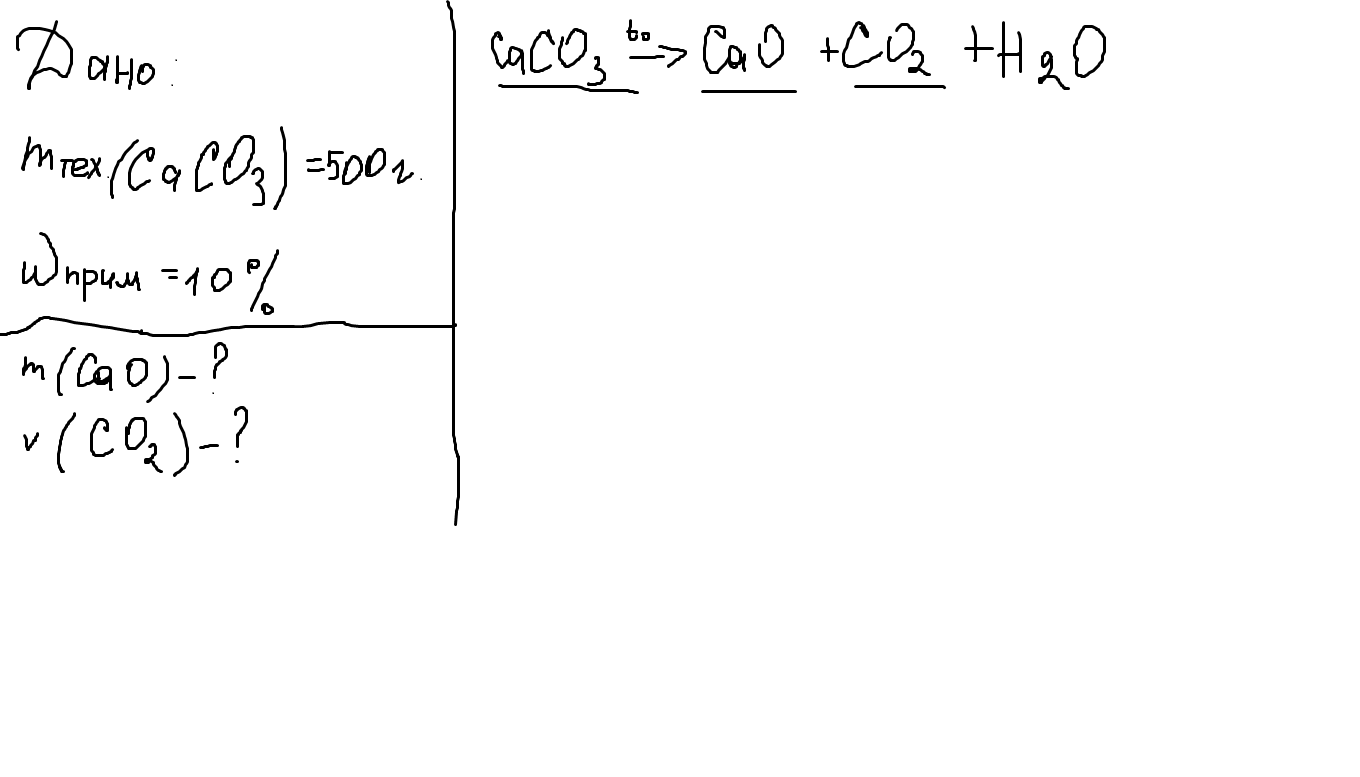
Объясните пожалуйста как решать задачи на примеси.
1
ответ
Вода в вашем уравнении совершенно лишняя. потому как в левой части водорода нет совсем, а по закону сохранения вещества взятся ему совершенно неоткуда.
Это было лирическое отступление.
Сейчас, собственно, к задаче.
Разложение карбоната кальция:
СаСО3 = СаО + СО2
Раз дан технический карбонат и указана массовая доля примесей в нем, то находим массу чистого карбоната кальция.
Если массовая доля примесей равна 10%, то остальные 90% - это чистый карбонат кальция.
Значит, масса чистого карбоната кальция: m(CaCO3) = m(CaCO3 тех)*W(CaCO3) = (500*90%)/100% = 450 (г).
Вот и получаем, что разлагается у нас 450 г карбоната кальция.
Далее, решение идет как обычно.
Находим химическое количество карбоната кальция:
n(CaCO3) = m(CaCO3)/M(CaCO3) = 450/100 = 4,5 моль
Находим массу оксида кальция:
По уравнению реакции:
n(CaO) = n(CaCO3) = 4,5 моль
m(CaO) = n(CaO)*M(CaO) = 4,5*56 = 252 г
Находим объем оксида углерода:
По тому же уравнению:
n(CO2) = n(CaCO3) = 4,5 моль
V(CO2) = n(CO2)*Vm = 4,5*22,4 = 100,8 л.
Это было лирическое отступление.
Сейчас, собственно, к задаче.
Разложение карбоната кальция:
СаСО3 = СаО + СО2
Раз дан технический карбонат и указана массовая доля примесей в нем, то находим массу чистого карбоната кальция.
Если массовая доля примесей равна 10%, то остальные 90% - это чистый карбонат кальция.
Значит, масса чистого карбоната кальция: m(CaCO3) = m(CaCO3 тех)*W(CaCO3) = (500*90%)/100% = 450 (г).
Вот и получаем, что разлагается у нас 450 г карбоната кальция.
Далее, решение идет как обычно.
Находим химическое количество карбоната кальция:
n(CaCO3) = m(CaCO3)/M(CaCO3) = 450/100 = 4,5 моль
Находим массу оксида кальция:
По уравнению реакции:
n(CaO) = n(CaCO3) = 4,5 моль
m(CaO) = n(CaO)*M(CaO) = 4,5*56 = 252 г
Находим объем оксида углерода:
По тому же уравнению:
n(CO2) = n(CaCO3) = 4,5 моль
V(CO2) = n(CO2)*Vm = 4,5*22,4 = 100,8 л.
0
·
Хороший ответ
4 апреля 2023 12:51
Остались вопросы?
Еще вопросы по категории Химия
Напишите пожалуйста изомеры Уксусной кислоты....
Подскажите,пожалуйста,CrO,CrO3 какие это оксиды?...
4.Составьте уравнения химических реакций по описанию: а)при взаимодействии оксида железа(III) Fe2O3 с водородом образуется железо и вода; б)хлор Cl2 в...
Назовите вещество...
NaHCO3 → Na2CO3 + H2O + CO2 Определить тип реакции...